14.02.2017, godzina 9:15, sala 1.03.
„Charakterystyka stabilności i reaktywności ludzkich metalotionein w kontekście komórkowej homeostazy jonów Zn(II)”.
mgr Agnieszka Drozd
Promotor: prof. dr hab. Artur Krężel
Zakład Chemii Biologicznej
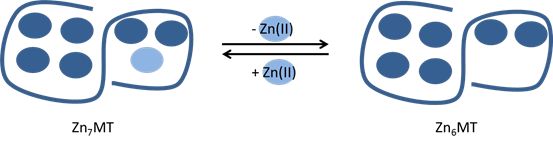
W pełni wysycona jonami Zn(II) metalotioneina (MT) tworzy Zn7MT kompleks. Siódmy jon Zn(II) związany przez metalotioneinę (jasny niebieski kolor) jest uważany za luźno związany i odpowiada za unikalne właściwości metalotioneiny do buforowania jonów Zn(II). Dzięki tym właściwościom, białko pełni rolę zarówno donora jak i akceptora jonów Zn(II) i uczestniczy w utrzymywaniu homeostazy jonów Zn(II) w komórce.









